Mikroskopie der Salze: Unterschied zwischen den Versionen
Ricon (Diskussion | Beiträge) |
Ricon (Diskussion | Beiträge) Keine Bearbeitungszusammenfassung |
||
| Zeile 27: | Zeile 27: | ||
== Bestimmung von Einzelsalzen aus dem wässrigen Auszug == | == Bestimmung von Einzelsalzen aus dem wässrigen Auszug == | ||
Vor den eigentlichen Salzbestimmung wird die zu untersuchuend | Vor den eigentlichen Salzbestimmung wird die zu untersuchuend Probe, ob Reinsalz oder Materialprobe mit wenigen Tropfen destilliertem Wasser versetzt und ein wässriger Auszug nach Bläuer erstellt. Von diesem wässrigen Auszug werden mehrere Tropfen auf einen Objektträger gebracht und unter dem Polarisationsmikroskop beobachtet. Wichtig ist, dass man die Auskristalisation der Salze aus der Lösung von Anfang an, also mit den ersten kleinen Kristallen, bis zum Ende der Krisatllisation beobachtet, da nur dann die richtigen Schlüsse gezogen werden können, da z.B zu Beginn auskrisatllisrende Salze durch nachfolgende komplett überdeckt und somit am Ende der Kristallisation kaum noch erkannt und bestimmt werden können. Von großer Bedeutung ist deshalb auch die Möglichkeit der kontinulierlichen Dokumentaion dessen, was man beobachtet. | ||
== Halit == | == Halit == | ||
In den Abbildungen 1-3 erkennen sie | In den Abbildungen 1-3 erkennen sie isotrope Halitkristalle, die neben KCL die einzigen isotopen und damit den kubischen Kristallsystem angehörenden Salze sind. Der Umkehrschluss gilt nicht, dass alle auf einem Objekträger isotrop erscheinen Kristalle auch kubisch sind wie Halit und Silvin, da mache Salze (vgl. Abb. ??), auf dem Objektträger derart orientiert auskrisallisieren, dass sie optisch isotrop erscheinen. Hier ist also Vorsicht geboten. Zusammen mit den typisch kubischen Kristallformen ist die Beobachtung jedoch eindeutig. | ||
| Zeile 42: | Zeile 42: | ||
== Calciumchlorid == | == Calciumchlorid == | ||
Calciumchlorid kristallisert nur bei relativ niederiger relativer Luftfeuchte (bei Reinsalzen bei RH < %RH) aus. Da die relative Luftfeuchte an den Objekten und auch im Laborraum meist über diesen | Calciumchlorid kristallisert nur bei relativ niederiger relativer Luftfeuchte (bei Reinsalzen bei RH < %RH) aus. Da die relative Luftfeuchte an den Objekten und auch im Laborraum meist über diesen Wert liegt, ist Calciumchlorid nur selten kristallin am Objekt zu beobachten. Um die Kristalle unter der Polarisationsmikroskop zu beobachten ist eine Möglichkeit, den Objektträger soweit zu erwärmen, bis sich Kristalle bilden, die sich jedoch beim Abkühlen rasch wieder in der Luftfeuchte lösen. In den Abbildungen XX sind Calciumchloridkristalle nach dem Erwärmen abgebildet. | ||
Version vom 9. Januar 2011, 21:06 Uhr
<bibimport />
Autoren: Hans-Jürgen Schwarz
zurück zu Verfahren zur Salzanalyse
Diese Seite ist in Bearbeitung und wird in Kürze freigeschaltet.
Abstract[Bearbeiten]
Die Bestimmung von Salzen mit einem Polarisationsmikroskop wird beschrieben.
Vorgehensweise[Bearbeiten]
Die Untersuchung von Salzen kann auf unterchiedliche Art erfolgen. Wichtig ist jedoch, dass immer sowohl die Anionen und Kationen bestimmt werden, wenn möglich auch die Phasen, das heist die Salze selbst. Bei der üblichen chemischen Analyse wird in der Regel das Carbonat-Ion nicht bestimmt, so dass auch die entsprechenden Salze dann oft nicht gefunden werden, obwohl sie in vielen Fällen die Hauptsalze sein können.
Zwei unterschiedliche Herangehensweisen zur mikroskopischen Salzanalyse werden hier vorgestellt.
Die eine Art der Untersuchung von Salzen bezieht sich auf die Analyse des Salzes an sich, so wie es vom Objekt als Salzktristall genommen wurde. Die andere Möglichkeit analysiert die aus einer wässrigen Lösung auskristallsierenden Salze, sei es indem man die Salzkristalle in Lösung bringt oder indem man einen wässrigen Auszug eines Baustoffes erstellt. Beides führt zu Salzkristallisationen, die im Folgenden beschrieben werden und sich je nach Salztyp mehr oder weniger unterscheiden können. Siehe hierzu auch das Kapitel Mikrochemie.
Bestimmung von Einzelsalzen aus dem wässrigen Auszug[Bearbeiten]
Vor den eigentlichen Salzbestimmung wird die zu untersuchuend Probe, ob Reinsalz oder Materialprobe mit wenigen Tropfen destilliertem Wasser versetzt und ein wässriger Auszug nach Bläuer erstellt. Von diesem wässrigen Auszug werden mehrere Tropfen auf einen Objektträger gebracht und unter dem Polarisationsmikroskop beobachtet. Wichtig ist, dass man die Auskristalisation der Salze aus der Lösung von Anfang an, also mit den ersten kleinen Kristallen, bis zum Ende der Krisatllisation beobachtet, da nur dann die richtigen Schlüsse gezogen werden können, da z.B zu Beginn auskrisatllisrende Salze durch nachfolgende komplett überdeckt und somit am Ende der Kristallisation kaum noch erkannt und bestimmt werden können. Von großer Bedeutung ist deshalb auch die Möglichkeit der kontinulierlichen Dokumentaion dessen, was man beobachtet.
Halit[Bearbeiten]
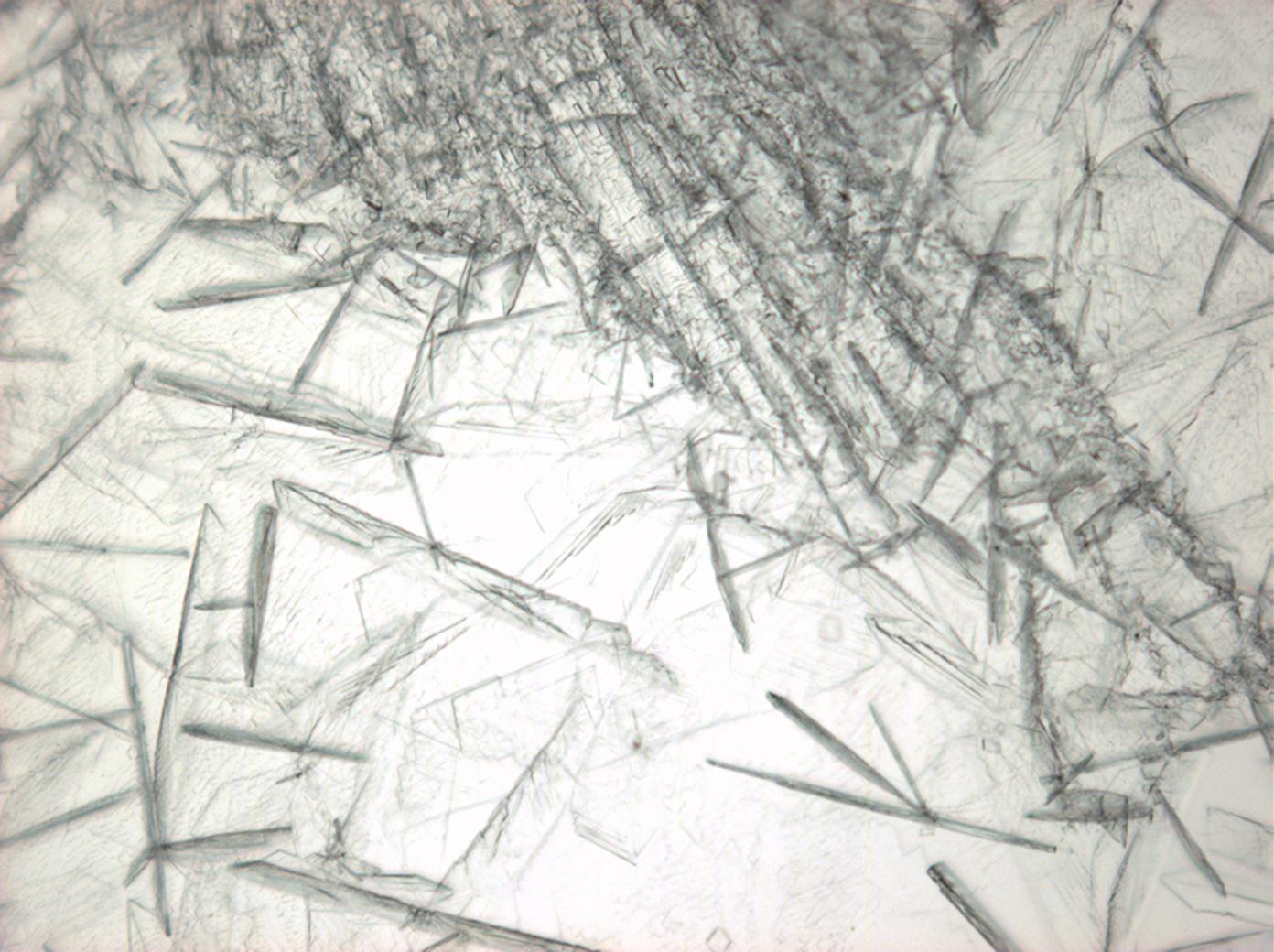
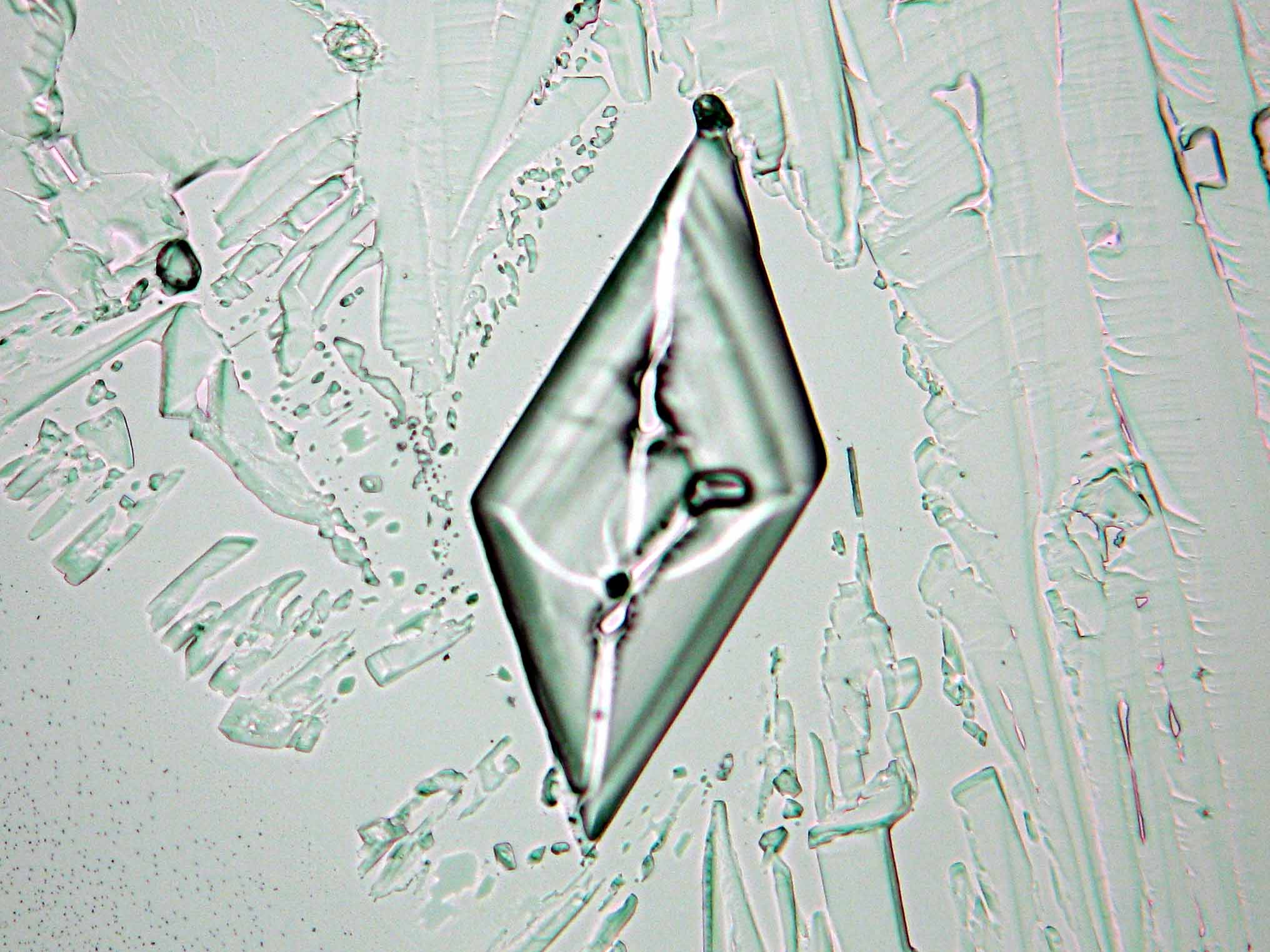
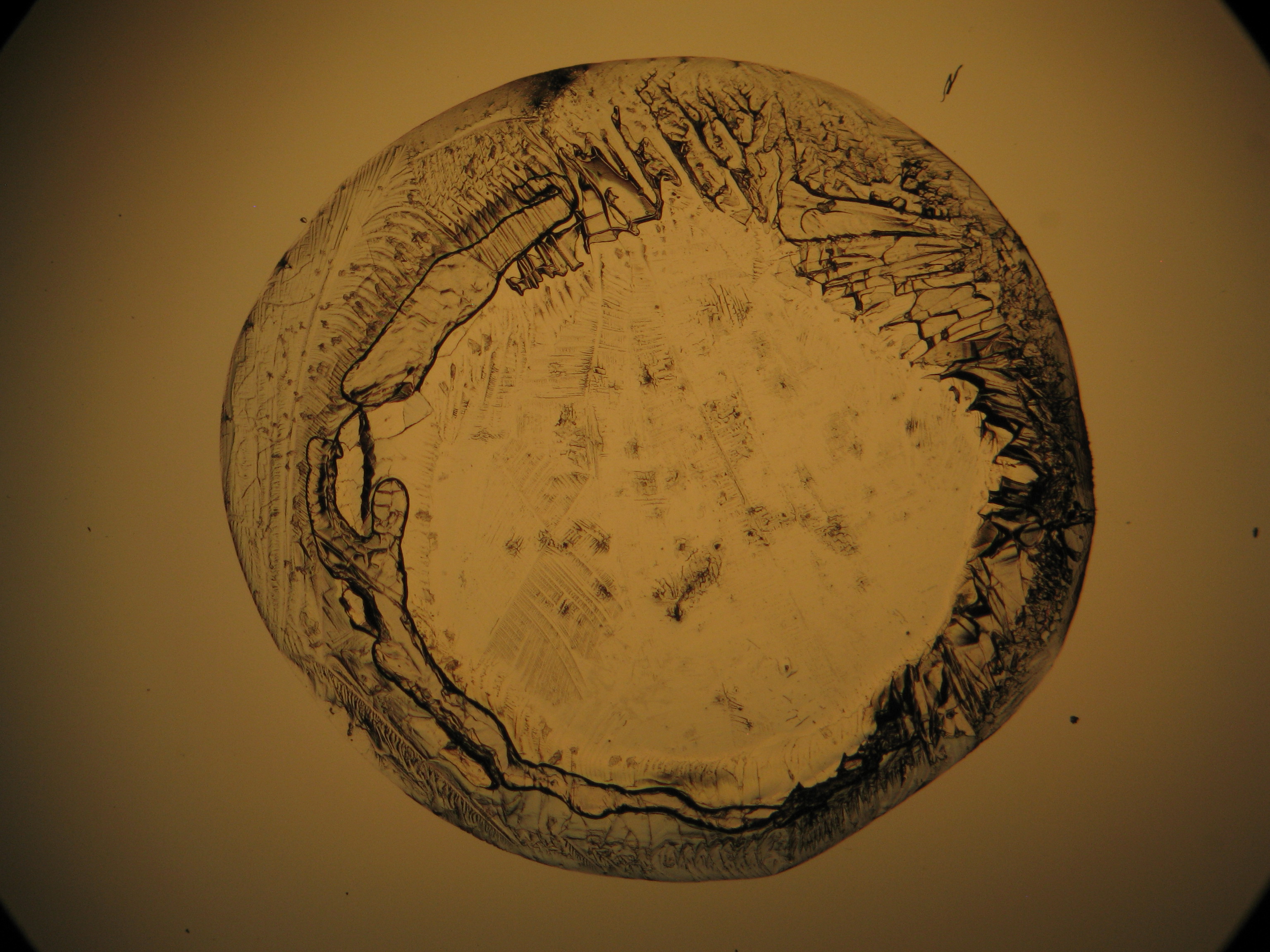
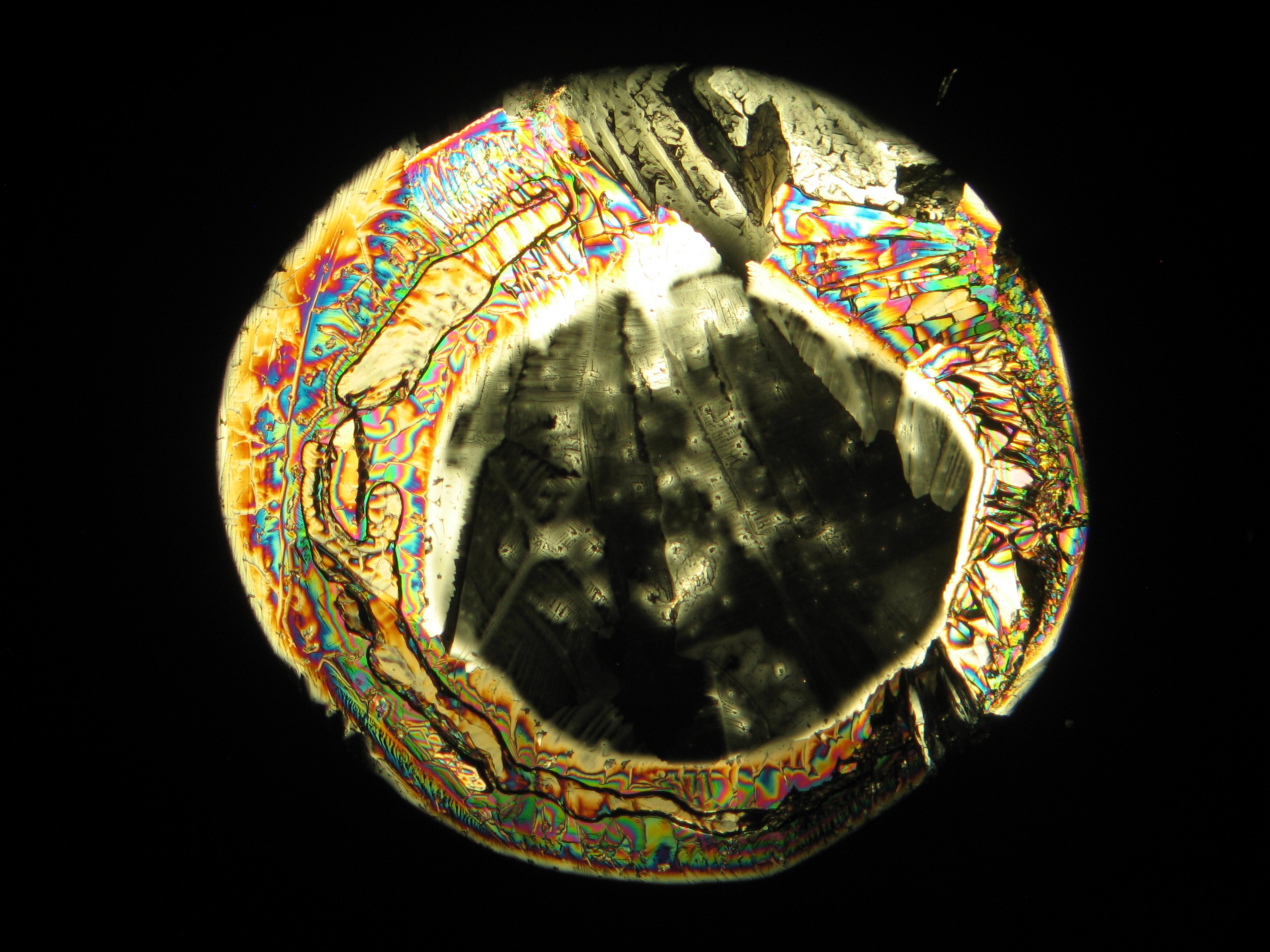
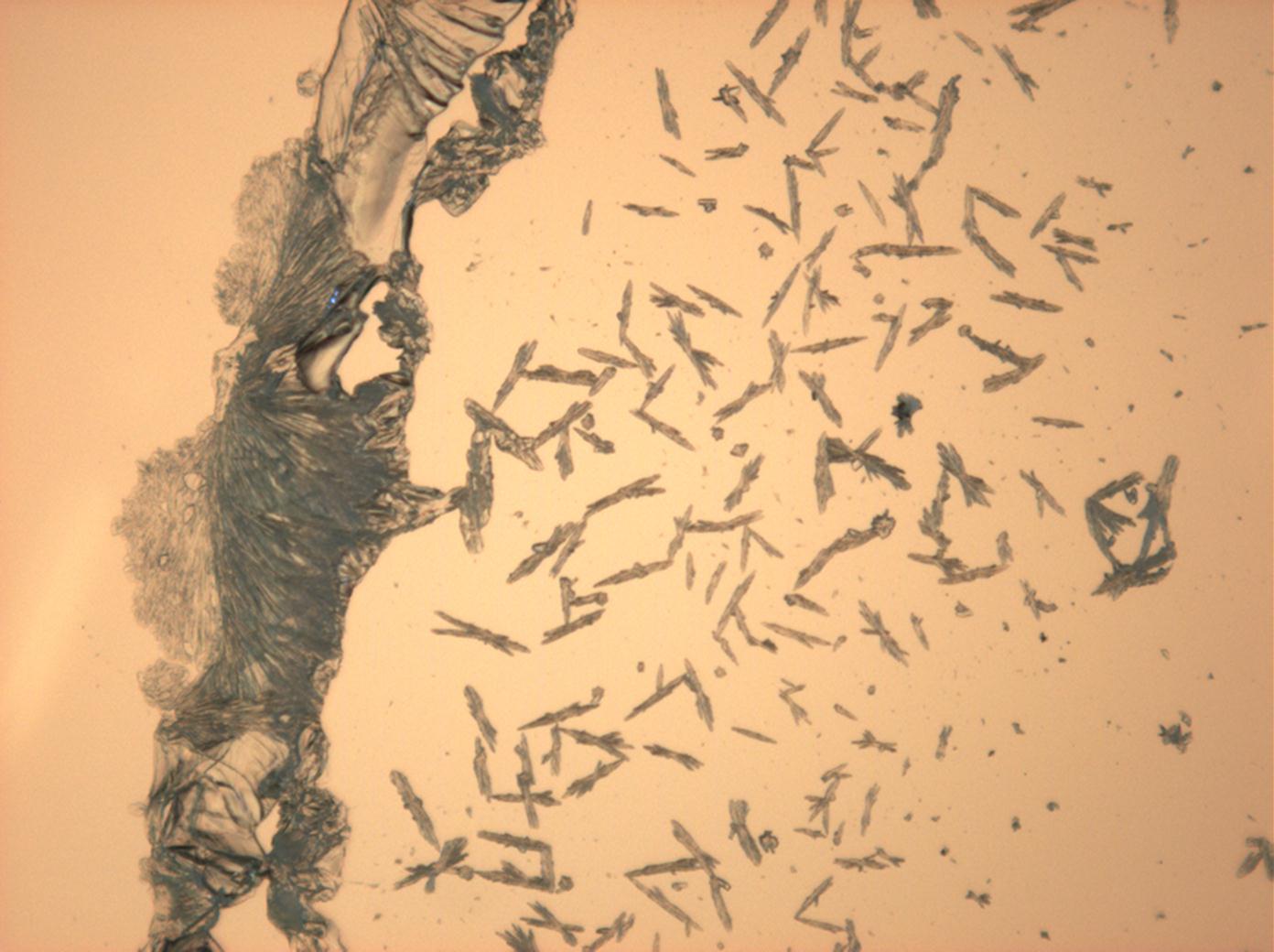
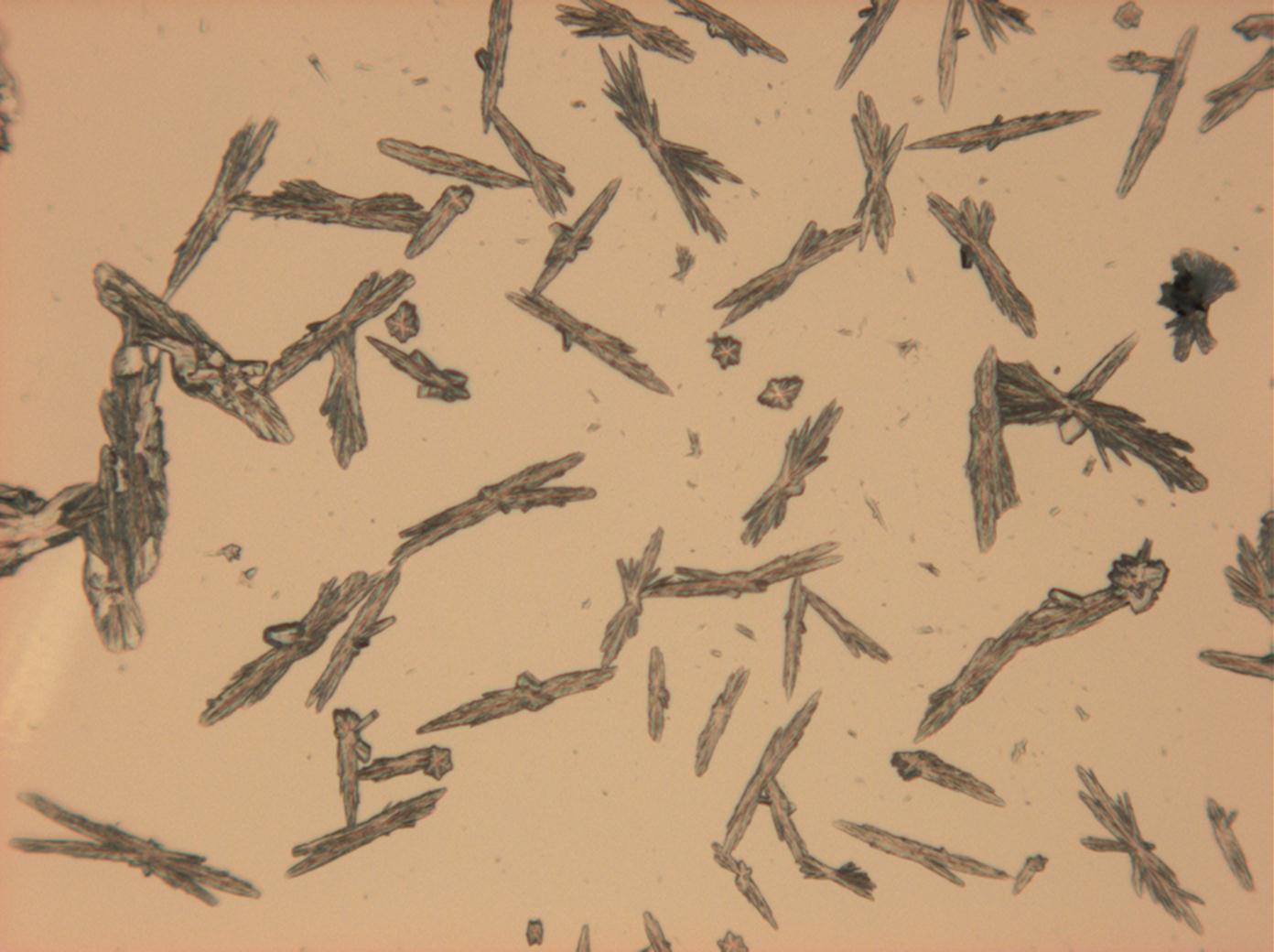
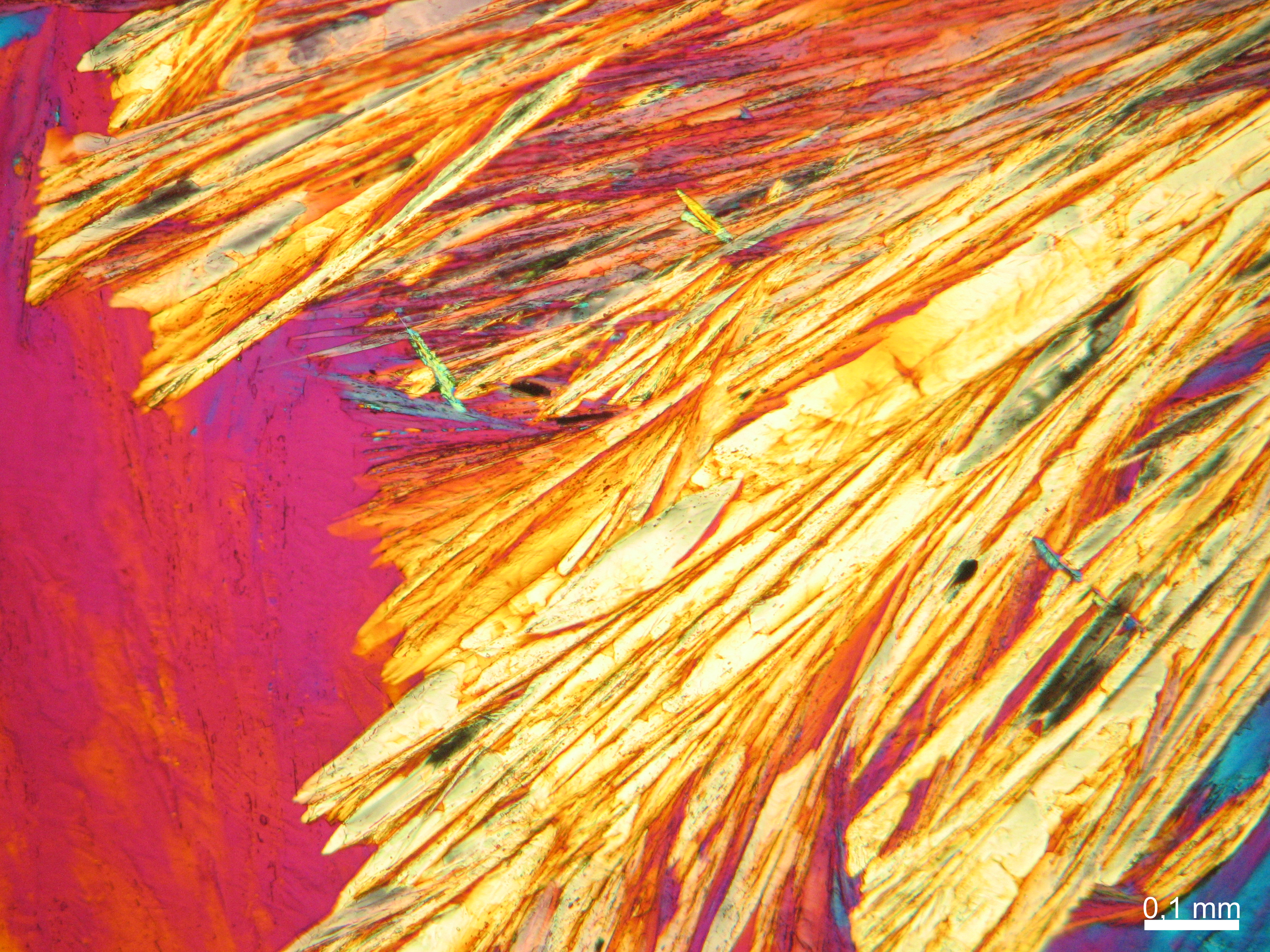
In den Abbildungen 1-3 erkennen sie isotrope Halitkristalle, die neben KCL die einzigen isotopen und damit den kubischen Kristallsystem angehörenden Salze sind. Der Umkehrschluss gilt nicht, dass alle auf einem Objekträger isotrop erscheinen Kristalle auch kubisch sind wie Halit und Silvin, da mache Salze (vgl. Abb. ??), auf dem Objektträger derart orientiert auskrisallisieren, dass sie optisch isotrop erscheinen. Hier ist also Vorsicht geboten. Zusammen mit den typisch kubischen Kristallformen ist die Beobachtung jedoch eindeutig.
- Halit aus wässriger Lösung auf einem Objektträger kristallisiert
Calciumchlorid[Bearbeiten]
Calciumchlorid kristallisert nur bei relativ niederiger relativer Luftfeuchte (bei Reinsalzen bei RH < %RH) aus. Da die relative Luftfeuchte an den Objekten und auch im Laborraum meist über diesen Wert liegt, ist Calciumchlorid nur selten kristallin am Objekt zu beobachten. Um die Kristalle unter der Polarisationsmikroskop zu beobachten ist eine Möglichkeit, den Objektträger soweit zu erwärmen, bis sich Kristalle bilden, die sich jedoch beim Abkühlen rasch wieder in der Luftfeuchte lösen. In den Abbildungen XX sind Calciumchloridkristalle nach dem Erwärmen abgebildet.
Tabelle mit den optischen Daten einfügen!!
- Calciumchlorid aus wässriger Lösung auf einem Objektträger kristallisiert
Niter[Bearbeiten]
- Niter aus wässriger Lösung auf einem Objektträger kristallisiert
Calciumnitrat[Bearbeiten]
- Calciumnitrat aus wässriger Lösung auf einem Objektträger kristallisiert
Magnesiumnitrat[Bearbeiten]
- Magnesiumnitrat aus wässriger Lösung auf einem Objektträger kristallisiert
Gips[Bearbeiten]
- Gips aus wässriger Lösung auf einem Objektträger kristallisiert
Magnesiumsulfat[Bearbeiten]
- Magnesiumsulfat aus wässriger Lösung auf einem Objektträger kristallisiert
Natriumsulfat[Bearbeiten]
- Natriumsulfat aus wässriger Lösung auf einem Objektträger kristallisiert
Natriumcarbonat[Bearbeiten]
- Natriumcarbonat aus wässriger Lösung auf einem Objektträger kristallisiert
Natriumacetat[Bearbeiten]
- Natriumacetat aus wässriger Lösung auf einem Objektträger kristallisiert