Sylvin: Unterschied zwischen den Versionen
Zur Navigation springen
Zur Suche springen
Keine Bearbeitungszusammenfassung |
|||
| (56 dazwischenliegende Versionen von 5 Benutzern werden nicht angezeigt) | |||
| Zeile 1: | Zeile 1: | ||
Autoren: | Autoren: [[Benutzer:Hschwarz|Hans-Jürgen Schwarz]], NN.... | ||
<br>zurück zu [[Chloride]] | |||
{{Infobox_Salz | |||
|Footnote=<ref>http://webmineral.com/data/Sylvite.shtml gesehen 29.07.2010</ref><ref>http://www.mindat.org/min-3850.html gesehen 29.07.2010</ref><ref>http://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Sylvin gesehen 29.07.2010</ref> | |||
|bild =[[Image:HJS KCl-111703-03-10x.jpg|300px]] | |||
|mineralogischerName=Sylvin | |||
|chemischerName =Kaliumchlorid | |||
|Trivialname = | |||
|chemFormel =KCl | |||
|Hydratformen = | |||
|Kristallsystem =kubisch | |||
|Deliqueszenzfeuchte =85,0% | |||
|Löslichkeit=4,595 mol/kg | |||
|Dichte =1,987 g/cm<sup>3</sup> | |||
|Molvolumen =37,52 cm<sup>3</sup>/mol | |||
|Molgewicht = 74,56 g/mol | |||
|Transparenz =durchsichtig | |||
|Spaltbarkeit =vollkommen | |||
|Kristallhabitus = | |||
|Zwillingsbildung = | |||
|Brechungsindices = n=1,4903 | |||
|Doppelbrechung = | |||
|optOrientierung=isotrop | |||
|Pleochroismus = | |||
|Dispersion = | |||
|Phasenübergang = | |||
|chemVerhalten = | |||
|Bemerkungen = | |||
|Literatur =<bib id="Steiger.etal:2014"/> <bib id="Robie.etal:1978"/> <bib id="Dana:1951"/> | |||
}} | |||
__TOC__ | |||
<!-- | |||
== Abstract == | |||
= <br>Einleitung = | |||
= <br>Allgemeines = | |||
== <br>Vorkommen von Silvin == | |||
= <br> | == <br>Angaben zu Herkunft und Bildung von Silvin an Baudenkmalen == | ||
<br> | |||
= <br> | = <br>Angaben zum Schadenspotential und zur Verwitterungsaktivität von Silvin = | ||
--> | |||
== Lösungsverhalten == | |||
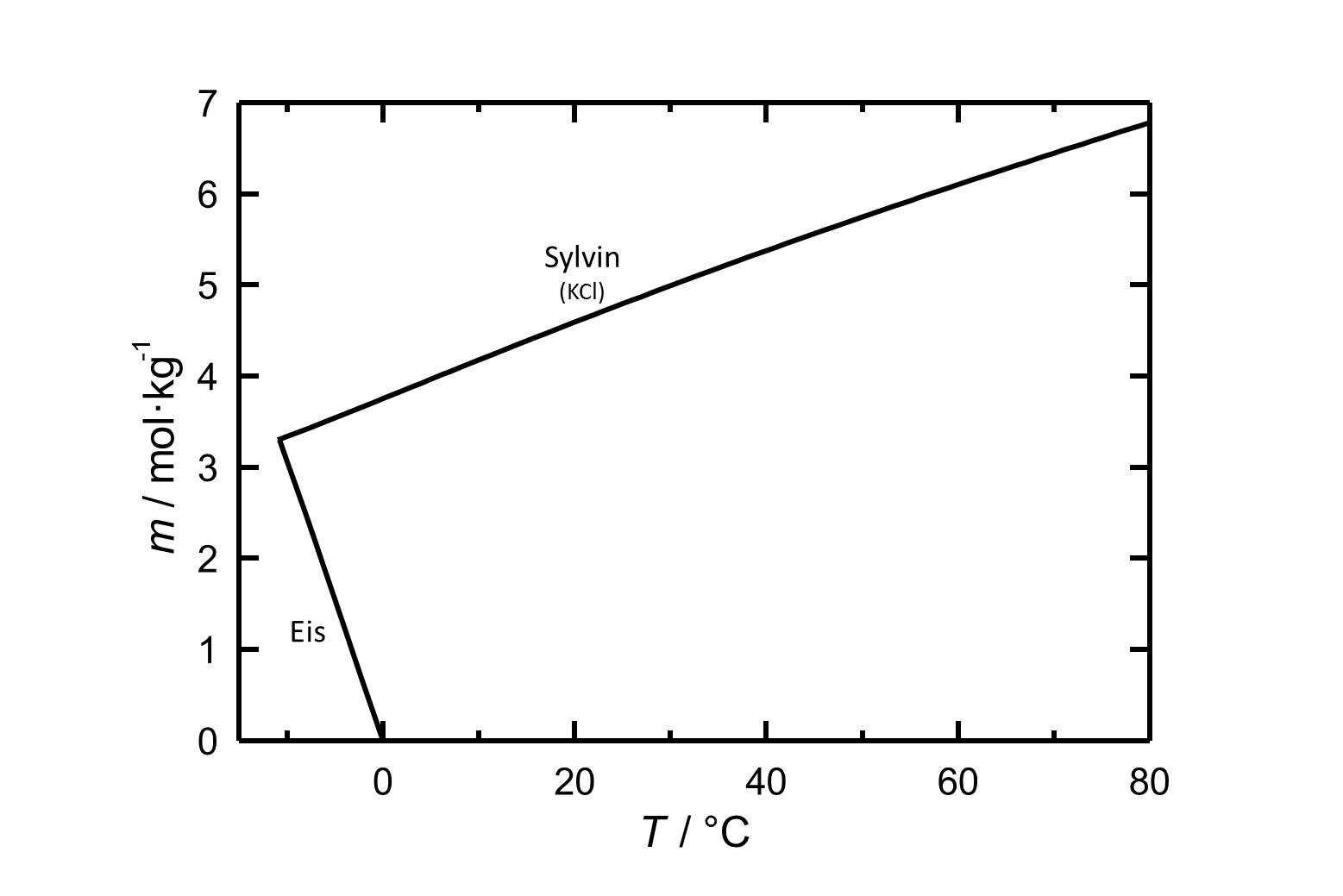
[[Image:L KCl d.jpg|800px|thumb|left|'''Abbildung 1''': Löslichkeit von Kaliumchlorid in Wasser. Aufgetragen ist die Molalität ''m'' [n(KCl)•kg(H<sub>2</sub>O)<sup>-1</sup>] gegen die Temperatur. Nach <bib id="Steiger.etal:2008c"/>]] | |||
<br clear=all> | |||
= | == Hygroskopizität == | ||
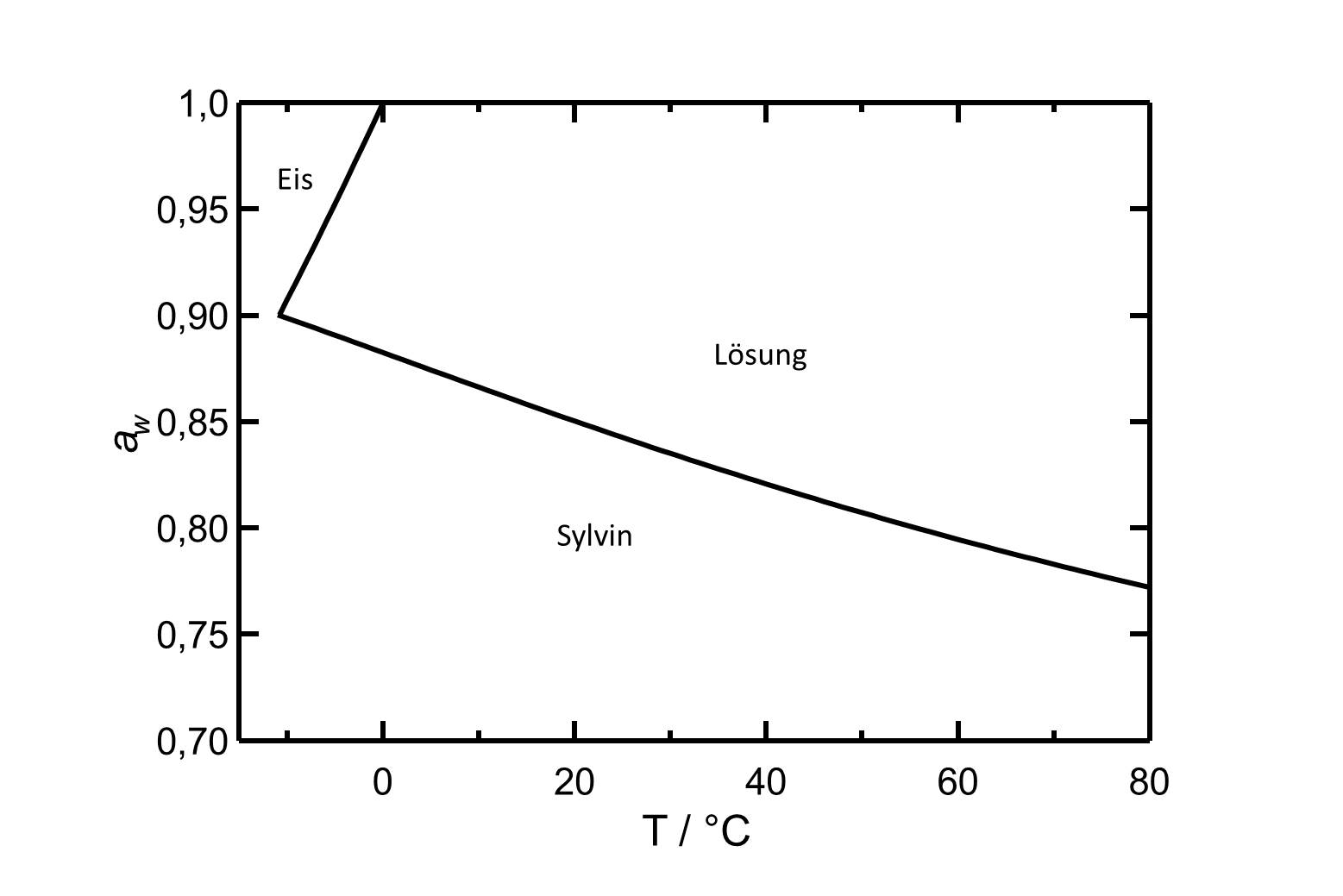
[[Image:D KCl d.jpg|800px|thumb|left|'''Abbildung 2''': Deliqueszenzverhalten von Kaliumchlorid in Abhängigkeit der Temperatur. Aufgetragen ist die Wasseraktivität ''a<sub>w</sub>'' gegen die Temperatur.]] | |||
<br clear=all> | |||
{| | |||
{|border="2" cellspacing="0" cellpadding="4" width="52%" align="left" class="wikitable" | |||
|+''Tabelle 1: Deliqueszenzfeuchte von Kaliumchlorid in Temperaturabhängigkeit nach <bib id="Steiger.etal:2014"/>'' | |||
|- | |- | ||
| | |bgcolor = "#F0F0F0" align=center| 0°C | ||
| | |bgcolor = "#F0F0F0" align=center| 10°C | ||
| | |bgcolor = "#F0F0F0" align=center| 20°C | ||
|bgcolor = "#F0F0F0" align=center| 30°C | |||
|bgcolor = "#F0F0F0" align=center| 40°C | |||
|bgcolor = "#F0F0F0" align=center| 50°C | |||
|- | |- | ||
| | |bgcolor = "#FFFFEO" align=center| 88,3%r.F. | ||
| | |bgcolor = "#FFFFEO" align=center| 86,7%r.F. | ||
| | |bgcolor = "#FFFFEO" align=center| 85,0%r.F. | ||
|bgcolor = "#FFFFEO" align=center| 83,5%r.F. | |||
|bgcolor = "#FFFFEO" align=center| 82,1%r.F. | |||
|bgcolor = "#FFFFEO" align=center| 80,7%r.F. | |||
|} | |} | ||
<br clear=all> | |||
<!-- | |||
[[Image:KCl a.jpg|thumb|center|400px]] | |||
'''Feuchtesorption:'''<br><br> | |||
== Kristallisationsdruck == | |||
<br> | <br> | ||
= <br>Analytischer Nachweis = | = <br>Analytischer Nachweis = | ||
| Zeile 141: | Zeile 99: | ||
'''Laboruntersuchung:''' <br> | '''Laboruntersuchung:''' <br> | ||
<br> | |||
'''Brechungsindex:''' n<sub>D</sub> = | '''Brechungsindex:''' n<sub>D</sub> = <br>'''Kristallklasse:''' kubisch<br> | ||
'''Polarisationsmikroskopische Untersuchung:''' | '''Polarisationsmikroskopische Untersuchung:''' | ||
<br> | |||
<br> '''Verwechslungsmöglichkeiten:'''<br> | <br> '''Verwechslungsmöglichkeiten:'''<br> | ||
<br> | |||
<br> | <br> | ||
| Zeile 160: | Zeile 116: | ||
|- | |- | ||
| '''Salzphase''' | | '''Salzphase''' | ||
| <font color="#818181"> '''Unterscheidungsmerkmale zu | | <font color="#818181"> '''Unterscheidungsmerkmale zu '''</font> | ||
|- | |- | ||
| | | <br> | ||
| | | <br> | ||
|- | |- | ||
| | | <br> <sub></sub> | ||
| | | <br> | ||
|} | |} | ||
| Zeile 179: | Zeile 135: | ||
== <br>IR-Spektroskopie == | == <br>IR-Spektroskopie == | ||
= <br>Umgang mit | = <br>Umgang mit Silvinschäden = | ||
--> | |||
<br clear=all> | |||
<!-- | |||
=== Am Objekt === | |||
--> | |||
== Unter dem Polarisationsmikrokop == | |||
= | <gallery caption="in einfach polarisiertem Licht" widths="200px" heights="200px" perrow="3"> | ||
Image:HJS KCl 100903-10-4.jpg | | |||
Image:HJS KCl 100903-10-1.jpg | | |||
Image:HJS KCl-111703-03-10x.jpg| | |||
Image:HJS KCl 100903-10-2.jpg | | |||
</gallery> | |||
<br> | <br> | ||
== | <gallery caption="unter gekreuzten Polarisatoren (Rot I)" widths="200px" heights="200px" perrow="3"> | ||
Image:HJS KCl 100903-10-3.jpg | |||
Image: | |||
Image: | |||
< | </gallery> | ||
<!-- | |||
=== Unter dem Rasterelektronenmikroskop === | |||
--> | |||
== Weblinks == | |||
<references /> | |||
== Literatur == | |||
<biblist/> | |||
[[Category: | [[Category:Silvin]] [[Category:Schwarz,Hans-Jürgen]] [[Category:R-MSteiger]] [[Category:Bearbeitung]][[Category:Chlorid]][[Category:Salz]][[Category:Liste]] | ||
Aktuelle Version vom 17. März 2015, 13:50 Uhr
Autoren: Hans-Jürgen Schwarz, NN....
zurück zu Chloride
| Sylvin[1][2][3] | |

| |
| Mineralogische Salzbezeichnung | Sylvin |
| Chemische Bezeichnung | Kaliumchlorid |
| Trivialname | |
| Chemische Formel | KCl |
| Hydratformen | |
| Kristallsystem | kubisch |
| Deliqueszenzfeuchte 20°C | 85,0% |
| Löslichkeit(g/l) bei 20°C | 4,595 mol/kg |
| Dichte (g/cm³) | 1,987 g/cm3 |
| Molares Volumen | 37,52 cm3/mol |
| Molare Masse | 74,56 g/mol |
| Transparenz | durchsichtig |
| Spaltbarkeit | vollkommen |
| Kristallhabitus | |
| Zwillingsbildung | |
| Phasenübergang | |
| Chemisches Verhalten | |
| Bemerkungen | |
| Kristalloptik | |
| Brechungsindices | n=1,4903 |
| Doppelbrechung | |
| Optische Orientierung | isotrop |
| Pleochroismus | |
| Dispersion | |
| Verwendete Literatur | |
| [Steiger.etal:2014]Titel: Weathering and Deterioration Autor / Verfasser: Steiger, Michael; Charola A. Elena; Sterflinger, Katja  [Robie.etal:1978]Titel: Thermodynamic properties of minerals and related substances at 298.15 K and 1 bar pressure and higher temperatures [Robie.etal:1978]Titel: Thermodynamic properties of minerals and related substances at 298.15 K and 1 bar pressure and higher temperaturesAutor / Verfasser: Robie R.A., Hemingway B.S.; Fisher J.A.  [Dana:1951]Titel: Dana's System of Mineralogy [Dana:1951]Titel: Dana's System of MineralogyAutor / Verfasser: Dana J.D. 
| |
Lösungsverhalten[Bearbeiten]

Abbildung 1: Löslichkeit von Kaliumchlorid in Wasser. Aufgetragen ist die Molalität m [n(KCl)•kg(H2O)-1] gegen die Temperatur. Nach [Steiger.etal:2008c]Titel: An improved model incorporating Pitzer's equations for calculation of thermodynamic properties of pore solutions implemented into an efficient program code
Autor / Verfasser: Steiger, Michael; Kiekbusch, Jana; Nicolai, Andreas

Autor / Verfasser: Steiger, Michael; Kiekbusch, Jana; Nicolai, Andreas

Hygroskopizität[Bearbeiten]
| 0°C | 10°C | 20°C | 30°C | 40°C | 50°C |
| 88,3%r.F. | 86,7%r.F. | 85,0%r.F. | 83,5%r.F. | 82,1%r.F. | 80,7%r.F. |
Unter dem Polarisationsmikrokop[Bearbeiten]
- in einfach polarisiertem Licht
- unter gekreuzten Polarisatoren (Rot I)
Weblinks[Bearbeiten]
- ↑ http://webmineral.com/data/Sylvite.shtml gesehen 29.07.2010
- ↑ http://www.mindat.org/min-3850.html gesehen 29.07.2010
- ↑ http://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Sylvin gesehen 29.07.2010
Literatur[Bearbeiten]
| [Dana:1951] | Dana E.S. (Hrsg.) Dana J.D. (1951): Dana's System of Mineralogy, 7, Wiley & Sons |  |
| [Robie.etal:1978] | Robie R.A., Hemingway B.S.; Fisher J.A. (1978): Thermodynamic properties of minerals and related substances at 298.15 K and 1 bar pressure and higher temperatures. In: U.S. Geol. Surv. Bull, 1452 () |  |
| [Steiger.etal:2008c] | Steiger, Michael; Kiekbusch, Jana; Nicolai, Andreas (2008): An improved model incorporating Pitzer's equations for calculation of thermodynamic properties of pore solutions implemented into an efficient program code. In: Construction and Building Materials, 22 (8), 1841-1850, Webadresse, https://doi.org/10.1016/j.conbuildmat.2007.04.020 |  |
| [Steiger.etal:2014] | Steiger, Michael; Charola A. Elena; Sterflinger, Katja (2014): Weathering and Deterioration. In: Siegesmund S.; Snethlage R. (Hrsg.): Stone in Architecture, Springer Verlag Berlin Heidelberg, 223-316, Webadresse, https://doi.org/10.1007/978-3-642-45155-3_4. |  |