Thenardit: Unterschied zwischen den Versionen
(Die Seite wurde neu angelegt: „{| align="right" style="border: 2px solid rgb(224, 224, 224); padding: 5px; width: 380px; background-color: rgb(249, 249, 249);" |- | bgcolor="#cccccc" align="cen…“) |
Keine Bearbeitungszusammenfassung |
||
| Zeile 17: | Zeile 17: | ||
| bgcolor="#99ffaa" | Na<sub>2</sub>SO<sub>4</sub> | | bgcolor="#99ffaa" | Na<sub>2</sub>SO<sub>4</sub> | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| | | Hydratformen | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | | ||
Mirabilit ( | Mirabilit (Na<sub>2</sub>SO<sub>4</sub> • 10H<sub>2</sub>O), Natriumsulfatheptahydrat (Na<sub>2</sub>SO<sub>4</sub> • 7H<sub>2</sub>O) | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Kristallklasse | | Kristallklasse | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | orthorhombisch | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Deliqueszenzfeuchte 20°C | | Deliqueszenzfeuchte 20°C | ||
| Zeile 29: | Zeile 29: | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Dichte (g/cm³) | | Dichte (g/cm³) | ||
| bgcolor="#99ffaa" | 2, | | bgcolor="#99ffaa" | 2,7 | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Molvolumen | | Molvolumen | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | 53,11cm<sup>3</sup>/mol | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Molgewicht | | Molgewicht | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | 142,04g/mol | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Transparenz | | Transparenz | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Spaltbarkeit | | Spaltbarkeit | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Kristallhabitus | | Kristallhabitus | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Zwillingsbildung | | Zwillingsbildung | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Brechungsindices | | Brechungsindices | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | nx = 1,468; n<sub>y</sub> = 1,473; n<sub>z</sub> = 1,483 | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Doppelbrechung | | Doppelbrechung | ||
| bgcolor="#99ffaa" | Δ = 0, | | bgcolor="#99ffaa" | Δ = 0,015 | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Optische Orientierung | | Optische Orientierung | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | <br> | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Pleochroismus | | Pleochroismus | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | <br> | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Dispersion | | Dispersion | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | <br> | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Phasenübergang | | Phasenübergang | ||
| Zeile 68: | Zeile 68: | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Chemisches Verhalten | | Chemisches Verhalten | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | <br> | ||
|- bgcolor="#dddddd" | |- bgcolor="#dddddd" | ||
| Bemerkungen | | Bemerkungen | ||
| bgcolor="#99ffaa" | | | bgcolor="#99ffaa" | in wasserfreiem Ethanol unlöslich, löslich in Glycerin | ||
|} | |} | ||
| Zeile 205: | Zeile 205: | ||
== Unter dem Polarisationsmikrokop == | == Unter dem Polarisationsmikrokop == | ||
<gallery | <gallery caption="Auf dem Objektträger rekristallisiert" widths="200px" heights="200px" perrow="3"> | ||
Image:Gips-1.jpg | Gipskristalle unter polarisiertem Licht | Image:Gips-1.jpg | Gipskristalle unter polarisiertem Licht | ||
| Zeile 215: | Zeile 215: | ||
<br> | <br> | ||
<gallery | <gallery caption="Im Dünnschliff von Objektproben" widths="200px" heights="200px" perrow="3"> | ||
Image:Per_270603_5-13_14.jpg|Gipsgeschädigter Ziegel, St. Jakobi Perleberg | Image:Per_270603_5-13_14.jpg|Gipsgeschädigter Ziegel, St. Jakobi Perleberg | ||
| Zeile 225: | Zeile 225: | ||
== Unter dem Rasterelektronenmikroskop == | == Unter dem Rasterelektronenmikroskop == | ||
<gallery | <gallery caption="Im Rasterelektronenmikoskop" widths="180px" heights="200px" perrow="4"> | ||
Image:CaSO4-REM-SG2-1.jpeg | Gipskristalle im REM | Image:CaSO4-REM-SG2-1.jpeg | Gipskristalle im REM | ||
Version vom 19. September 2009, 11:39 Uhr
| Thenardit | |
| [[Image:{{{bild}}}|300px]] | |
| Mineralogische Salzbezeichnung | Thenardit |
| Chemische Bezeichnung | Natriumsulfat |
| Trivialname | Makit, Menardit, Pyrotechnit |
| Chemische Formel | Na2SO4 |
| Hydratformen |
Mirabilit (Na2SO4 • 10H2O), Natriumsulfatheptahydrat (Na2SO4 • 7H2O) |
| Kristallklasse | orthorhombisch |
| Deliqueszenzfeuchte 20°C | - |
| Dichte (g/cm³) | 2,7 |
| Molvolumen | 53,11cm3/mol |
| Molgewicht | 142,04g/mol |
| Transparenz | |
| Spaltbarkeit | |
| Kristallhabitus | |
| Zwillingsbildung | |
| Brechungsindices | nx = 1,468; ny = 1,473; nz = 1,483 |
| Doppelbrechung | Δ = 0,015 |
| Optische Orientierung | |
| Pleochroismus | |
| Dispersion | |
| Phasenübergang | - |
| Chemisches Verhalten | |
| Bemerkungen | in wasserfreiem Ethanol unlöslich, löslich in Glycerin |
Autoren: Hans-Jürgen Schwarz , Nils Mainusch, NN....
Abstract[Bearbeiten]
Gips ist eines der wichtigsten Salze, die an z. B. Bauwerken und Wandmalereien für Schäden verantwortlich sind. Vor allem außen exponierte Objekte leider unter Gipsschäden. Die Eigenschaften, die Schadenswikung, das Vorkommen und auch der Nachweis von Gips werden behandelt. Abbildungen, Mikroaufnahmen und Beispiele aus der Praxis ergänzen und veranschaulichen das Dargelegte.
Einleitung[Bearbeiten]
Gips ist eines der heute am häufigsten vorkomenden bauschädlichen Salze. Er kommt in unterschiedlichen Formen und Ausprägungen an fast allen Objekten am Außenbau vor und auch in Innenräumen ist er häufig zu finden.
Allgemeines[Bearbeiten]
Vorkommen von Gips
[Bearbeiten]
Als eines der am meisten verbreiteten Minerale entsteht Gips beim Ausfall aus wässrigen Lösungen bei Temperaturen unter ca. 40°C. Liegen erhöhte Temperaturen (> 60°C) einer Lösung vor, so wird direkt Anhydrit gebildet. In Form von Gesteinen sind beide Calciumsulfatformen häufig anzutreffen. Natürliche Vorkommen des Halbhydrates existieren nicht.
Gips findet sich als Vorkommen in Salzlagerstätten und in Salzwüsten, wo durch den Einschluß von Quarzpartikeln bei der Formierung des Kristalls häufig sogenannte Wüstenrosen entstehen. In Salzlagerstätten bilden Gips und Anhydrit zuweilen einen “Salzhut” aus, d.h. eine mächtige Materialschicht, die sich über anderen Salzvorkommen eines natürlichen Lagers befindet.
Künstlich hergestellter Gips entsteht u.a. im Zuge der Entschwefelung von Rauchgasen in Kraftwerken, in denen fossile Brennstoffe verwertet werden.
Angaben zu Herkunft und Bildung von Gips an Baudenkmalen
[Bearbeiten]
Die hohe Schadensrelevanz von Gips für Denkmale aus mineralischer Bausubstanz steht wesentlich in Zusammenhang mit der Umwandlungsreaktion Kalk zu Gips. Unter der Einwirkung von SOx-haltiger Luft in Verbindung mit Feuchte können auf diese Weise wichtige Materialkomponeneten von Bauwerken (Kalkmörtel, Verputz, calcitische Gesteine etc.) zu Gips entsprechend dem Chemismus: CaCO3 + H2SO4 → CaSO4 + H2O + CO2 umgewandelt werden.
Gips stellt darüberhinaus einen wichtigen Baustoff für die Erstellung von Mörtel und Verputze dar und kann bereits als Gestein und somit originäres Baumaterial Eingang in das Gefüge eines Denkmals gefunden haben. Ähnliches gilt für Anhydrit.
Angaben zum Schadenspotential und zur Verwitterungsaktivität von Gips[Bearbeiten]
Lösungsverhalten[Bearbeiten]
Gips zählt zur Gruppe der “gering” (vgl.Tabelle Hygroskopizität der Salze und Gleichgewichtsfeuchte) wasserlöslichen Salze und kann somit als wenig mobil bezeichnet werden. Allerdings ist der Fremdioneneinfluß auf die Gipslöslichkeit vergleichsweise groß. So wird die Löslichkeit von Gips durch Halit je nach Konzentrationsverhältnis bis um den Faktor vier erhöht.
Diagramm 1 – Darstellung der temperaturabhängigen Veränderung der Löslichkeit von Gips im Vergleich mit anderen Salzphasen [Angaben nach Stark/Stürmer 1993].
Datei:Gips+NaCl Loeslichkeit.jpg
Diagramm 2 – Dargestellt ist die Veränderung der Löslichkeit von Gips in Wasser unter Anwesenheit von Halit. Liegt Halit in einer Konzentration von ca. 140 g/l in wäßriger Lösung vor, so lösen sich hierin etwa 8 g Gips. [Angaben nach J.D’Ans, 1933].
Hygroskopizität[Bearbeiten]
Gips besitzt als Reinsalz keinen definierten und durch die relative Feuchte beeinflussten Deliqueszenzpunkt. Bei Überschreiten von 90 % r.F. kann es in Gegenwart von Halit allerdings (durch die Feuchtesorption von Halit) zum Auflösen von Gipskristallen kommen; ein Absinken der Feuchtewerte auf ca.75 % r.F. bewirkt die Rekristallisation des Gipses [Angaben nach H.J.Schwarz, 1996].
Kristallisationsdruck[Bearbeiten]
Bei der Kristallisation aus wäßriger Lösung, die eine Übersättigung im Verhältnis 2:1 aufweist, läßt sich für Gips ein linearer Wachstumsdruck von 28,2-33,4 N/mm2 im Temperaturbereich 0-50°C angeben. Im Vergleich mit anderen bauschädlichen Salzen liegen diese Werte im mittleren Bereich einer berechneten Werteskala, die insgesamt von 7,2 bis 65,4 N/mm2 reicht [nach Winkler, 1975].
Hydratationsverhalten[Bearbeiten]
Das System CaSO4 – H2O:
Calciumsulfat kann in drei unterschiedlichen Hydratstufen auftreten, dem oben bezeichneten, kristallwasserlosen Anhydrit, einem Halbhydrat, welches unter Normalbedingungen die instabilste Form darstellt, und Gips. Anhydrit existiert in verschiedenen Modifikationen, wodurch je nach Abhängigkeit der Modifikation des vorliegenden Anhydrit unterschiedliche chemische Eigenschaften (z.B. variierende Löslichkeit in Wasser) feststellbar sind. Das gleiche gilt auch für die Modifikationen des Halbhydrates.
Als Wert für die Übergangstemperatur (in wäßriger Lösung) kann der Bereich 40°C-66°C angegeben werden. Unter normalen Klimabedingungen an Denkmalen entsteht somit beim Ausfall von Calciumsulfat aus einer wäßrigen Lösung in erster Linie Gips. Liegen die Temperatur einer Lösung höher als 40°C-60°C, bildet sich v.a. Anhydrit. Parallel hierzu kommt es zur Bildung des Halbhydrates, welches zwar metastabil ist, beim Ausfall aber zunächst in großer Menge auftritt und dann in eine der stabileren Hydratstufen umgebildet wird.
Bei der Erhitzung des Doppelhydrates (als Feststoff in Abwesenheit von wäßrigem Lösungsmittel) kommt es bei einer Temperatur ab etwa 50°C zum Austreiben von Kristallwasser, und es entsteht das Halbhydrat. Die vollständige Überführung zum Halbhydrat findet erst bei Temperaturen von ca. 100°C statt. Wird das Doppelhydrat längere Zeit auf 500-600°C erhitzt, liegt völlig entwässertes Calciumsulfat vor. Bei Temperaturen über 1000°C erfolgt die Zersetzung in Calciumoxid und SO3.
Hydratationsdruck[Bearbeiten]
An einem Objekt vorliegender Gips kann das im Molekül enthaltene Kristallwasser nur bei Temperaturen ab ca. 50°C abgeben, wird also in der Regel nicht dehydrieren. Umgekehrt ist die Einlagerung von Kristallwasser bei Vorliegen von Anhydrit oder Halbhydrat an einem Denkmal aber durchaus möglich. Beide Vorgänge sind mit Volumenveränderungen (von 31,9% beim Übergang Halbhydrat-Gips) und dem Entstehen von Hydratationsdrücken verbunden [Zahlenwerte nach Sperling/Cooke, 1980]. Für den Fall des Überganges Halbhydrat-Gips (Stichwort Gipstreiben) kann bei einer Temperatur im Bereich 0-20°C und einer r.F. von ca. 80% ein Hydratationsdruck von 114 –160 N/mm2 angegeben werden, was extrem hohe Werte darstellt [nach Stark/Stürmer 1996]<bibref>Stark.etal:1996</bibref>.
Umwandlungsreaktionen[Bearbeiten]
Wie erläutert hängt der substanzgefährdende Charakter von Gips v.a. mit der Umwandlungsreaktion Calcit-Gips zusammen. Aus Calcit gebildete Gipsmoleküle besitzen ein Volumen, welches das der ursprünglichen Calcitmoleküle um etwa 100% übersteigt. In diesem Zusammenhang ist als relevanter Schadensfaktor die Veränderung der Wasserlöslichkeit zu nennen. Calcit ist mit einer Wasserlöslichkeit von ca. 0,014g/l (20°C) schwerer löslich als Gips, so daß nach Umwandlung zu Gips ein deutlich wasserempfindlicheres System vorliegt.
Hingewiesen sei auf die Untersuchungen von Snethlage und Wendler [1998], die den Einfluß von Gips auf die hygrischen Längenänderungen eines bestimmten Sandsteinmaterials analysiert haben und die beobachtete Schadensbildung in erster Linie auf das veränderte Quellverhalten durch den Gipseinfluß erklären.
Analytischer Nachweis[Bearbeiten]
Mikroskopie
[Bearbeiten]
Laboruntersuchung:
Gips ist gering wasserlöslich, so daß gipshaltiges Probematerial beim Versetzen mit Aquadest. nur geringfügig in Lösung geht. Wird gipshaltiges Probematerial in Lösung gebracht, entstehen bei vorsichtigem Einengen des Lösungmitteltropfens im Zuge der Rekristallisation zunächst Einzelnadeln und zunehmend nadelige Gipsaggregate im Bereich des Saumes der Lösung. (alternativ kann Probematerial mit Salzsäure versetzt werden, was ebenfalls zur Bildung von Kristallnadeln führt). Im Vergleich zu anderen Salzen, die ebenfalls nadelig rekristallisieren können wie z.B. Natriumcarbonat, weisen Gipsnadeln eine deutlich geringere Länge auf.
Brechungsindizes: nx = 1.521; ny =1.523; nz =1.530
Doppelbrechung: Δ = 0.009
Kristallklasse: monoklin
Polarisationsmikroskopische Untersuchung:
Außer dem typischen, nadeligen Habitus von Gipskristallen (v.a. von rekristallisiertem Material) treten unterschiedliche morphologische Charakteristika auf, die bei der Identifikation von Gips hilfreich sind. Gipspartikel (in Rohprobematerial) zeigen sich häufig in Form von gerundeten Splittern und tafeligen Rhomboedern, an denen deutliche, innere Spaltflächen ablesbar sind. Darüber hinaus ist das Auftreten von Zwillingsformen sowohl bei lattigen Partikeln wie auch Tafeln und Plättchen typisch für Gips.
Die Zuweisung der Brechungsindizes erfolgen entsprechend der Immersionsmethode unter Verwendung von Medien mit den Indizes nD=1,518 und nD=1,53, wobei aufgrund der zumeist sehr kleinteiligen Partikel die Überprüfung des Schroeder van der Kolk- Schatten aussagekräftiger und sicherer ist, als der Becke-Linien Test.
Gipskristalle gehören zur Klasse der monoklinen Kristalle zeigen also je nach Ausrichtung des Einzelpartikels unter dem Mikroskop zum einen sowohl parallele, bzw. symmetrische Auslöschung, weisen v.a. jedoch eine charakteristische schiefe Achsenstellung in der Auslöschungsposition auf. An gut ausgebildeten Kristallrhomben ist diese schiefe Auslöschung zumeist klar meßbar.
Von allen Calciumsulfaten ist Gips am geringsten doppelbrechend und erscheint bei gekreuzten Polarisatoren mit sehr niedrigen Interferenzfarben, die (natürlich in Abhängigkeit der vorliegenden Partikeldicke) im Bereich grau bis gelblich weiß der ersten Ordnung liegen.
Verwechslungsmöglichkeiten:
Gips ist im dargestellten Analyseverfahren eindeutig zuweisbar, sofern die folgenden Untersuchungskriterien eindeutig geklärt sind:
- geringe Wasserlöslichkeit
- charakteristisch nadelige Morphologie bei rekristallisierten Partikeln
- alle beobachtbaren Indizes besitzen einen nD –Wert zwischen 1,518 und 1,530
- Gipskristalle besitzen eine geringe Doppelbrechung und niedrige Interferenzfarben
- Gipskristalle weisen eine schiefe Auslöschung auf
Salzphasen, die gipsähnliche chemische und optische Eigenschaften aufweisen, sind nachstehend
aufgelistet:
| Salzphase | Unterscheidungsmerkmale zu Gips |
| Syngenit; K2Ca(SO4)•2H2O | alle beobachtbaren Indizes < 1,518 |
| Tachyhydrit; CaMg2Cl6•12H2O | zumeist ein beobachtbarer Index < 1,518 / nur parallele und symmetrische Auslöschung |
| Hydromagnesit; Mg5[OH(CO3)2]2•4H2O | ein Index zumeist > 1,53 |
Röntgendiffraktometrie[Bearbeiten]
Raman-Stektroskopie[Bearbeiten]
DTA/TG[Bearbeiten]
IR-Spektroskopie[Bearbeiten]
Umgang mit Gipsschäden[Bearbeiten]
Salze und Salzschäden im Bild[Bearbeiten]
Am Objekt[Bearbeiten]
Unter dem Polarisationsmikrokop[Bearbeiten]
- Auf dem Objektträger rekristallisiert
- Gips-1.jpg
Gipskristalle unter polarisiertem Licht
- Gips-2.jpg
Gipskristalle unter polarisiertem Licht, Rot I
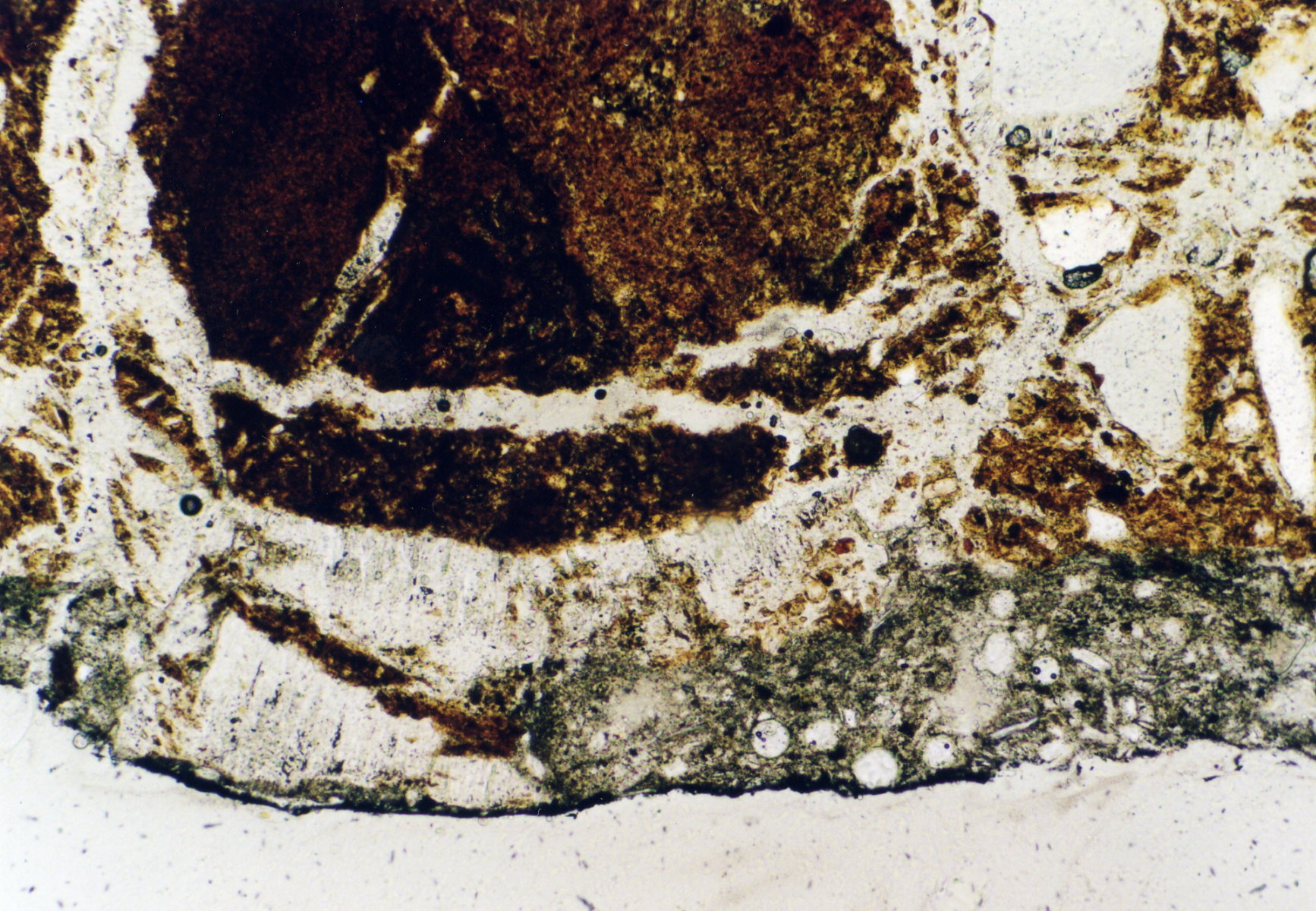
- Im Dünnschliff von Objektproben
- Per 270603 5-13 16.jpg
Gipsgeschädigter Ziegel, St. Jakobi Perleberg
Unter dem Rasterelektronenmikroskop[Bearbeiten]
- Im Rasterelektronenmikoskop
- CaSO4-REM-SG2-1.jpeg
Gipskristalle im REM
- CaSO4-REM-SG2-2.jpeg
Gipskristalle im REM
- CaSO4-REM-SG2-3.jpeg
Gipskristalle im REM
- CaSO4-REM-SG2-SPC.jpeg
Gipskristalle im REM
- CaSO4-REM-SG3-1.jpeg
Gipskristalle im REM
- CaSO4-REM-SG3-2.jpeg
Gipskristalle im REM
- CaSO4-REM-SG3-3.jpeg
Gipskristalle im REM
- CaSO4-REM-SG3-SPC2.jpeg
Gipskristalle im REM
Weblinks
[Bearbeiten]
http://webmineral.com/data/Gypsum.shtml
http://www.mindat.org/min-1784.html
http://www.mineralienatlas.de/lexikon/index.php/MineralData?mineral=Gips
Literatur[Bearbeiten]
<bibreferences/>